SARS-CoV-2 研究用試薬の展望
近畿本部 化学部会 12月講演会
日 時 :2021年12月11日(土) 14:00~17:00
場 所 :近畿本部会議室 + オンライン(Teams)
講演2 :
SARS-CoV-2 研究用試薬の展望
講師:飯塚 洋人 氏(生物工学、富士フイルム和光純薬株式会社)
(1)基本原理とSARS-CoV-2ウイルス構造
SARS-CoV-2とは、新型コロナウイルス感染症COVID-19の原因であるRNAウイルスをいう。DNAが転写されmRNA(メッセンジャーRNA)ができ、更に翻訳されたものがmRNAワクチンとして働きタンパク質と結合する。SARS-CoV-2ウイルスは、新型コロナウイルス感染症(COVID-19)の原因ウイルスであり、直径は約0.1μm、約29,903b(塩基)のRNAゲノムを持つ。スパイクタンパク質は細胞内テール膜貫通アンカー、レセプター結合S1サブユニット、膜融合S2サブユニットからなる。そのスパイクタンパク質のS1サブユニットには上皮細胞表面レセプターのアンデギオ転身変換酵素に結合するドメインが存在する。
(2)PCR検査
PCR (Polymerase
Chain Reaction)検査は、ポリメラーゼ連鎖反応によりウイルスを検出する方法である。PCR検査の際には、mRNA、tRNA(トランスファーRNA)がPCRで増幅され、DNAに逆転写により新型コロナウイルスが検出される。 SARS-CoV-2変異株検出用キットを用いて、RNA配列変異を検出する。また、変異株の種類に応じて設計した試薬を供給することが必須になる。PCRは、2本鎖DNAを熱変性させ一本鎖にし、短いDNA分子(プライマー)を、標的DNAに結合させ、耐熱性ポリメラーゼにより合成させ、1対のDNAが20サイクルで100万対まで増幅し、DNAが見えるまで増加することにより微量の新型コロナウイルスを検出できる。
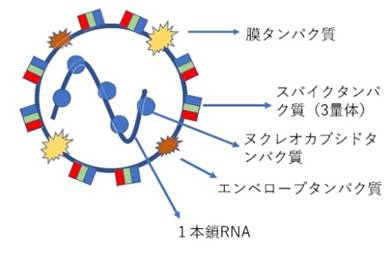 図1:SARS-CoV-2ウイルスの構造
図1:SARS-CoV-2ウイルスの構造
RNAを定量化する技術としてRT-PCR法がある。PCR増幅サイクルにより陽性の検体がある場合、RNA数を定量し陽性閾値を定め、陽性か陰性かを判定する。判明した標準品から検量線を作成し、未知のウイルスRNAを定量化できるが、変異株が増えたことによりマルチ式の高機能の検出器でなければ検査対応ができなくなる。
(3)mRNAワクチンとアデノウイルスワクチン
mRNAとは、4284個のヌクレオチド残基からなる1本鎖RNAをいう。mRNAは鋳型DNAのインビトロ転写反応後、二重鎖RNAを除去し、精製することにより得られる。1-メチルシュードウリジンを合成原料に使用しており、研究室レベルのものが実用化され、プラスミドの製造、自己複製型ワクチンの受託製造がある。
アデノウイルスは、遺伝子組み換え規制法(カルタヘルナ法)の第一種使用に該当し、構造は36kbp(塩基対)の2本鎖直鎖状プラスミドDNAをウイルスゲノムとして持ち20面体構造であり、表面を覆う膜を持たない。また、ヒト胎児腎細胞293(HEK293)細胞を用いて、組み換えアデノウイルス粒子を産出することにより、工業的にウイルスを合成できる。
新規モダリティについて、約30年前の遺伝子治療技術を転用し、ワクチンとして実用化され、例としてmRNA、アデノウイルスワクチン、自己複製型次世代ワクチンがある。
(4)今後の展望
オミクロン株(変異株)が新たに報告され、パンデミックは世界的に未だ収束していないことから、ワクチン製造のためにmRNAワクチン用のシュードウリジン、RNAポリメラーゼなどの合成原料の需要は高まる。現在、ワクチンは低温保存が必要であり、熱帯地域でのワクチンの需要を考慮すると耐熱性を持ったワクチンも必要になると考えられる。
Q&A
Q 創薬・新規モビリティについて、ディープラーニングの観点も含め、ワクチン創薬の基本的なテクノロジーを教えていただきたい。
A プライマーの設計の上での親和性―の高さについて、コンピュータで解析できると思われる。
抗体薬品に関しても、アミノ酸配列の結合のしやすさについてもAIを使った設計がおこなわれているのではないかと考えられる。
Q 試薬事業から見て、ウイルス研究に適する試薬を提供する立場から考えると、受注して生産するのか?ある程度予測して、薬品を品揃えするのか?また、どのようにウイルス研究し、試薬事業を展開しているのか?
A 市場予測での供給がメインになっている。当然、要求される試薬もあるが、予測してある程度試薬の在庫を増やす。スパイクタンパク質の種類があるので、あらかじめ準備し、試薬を供給できるようにしておく。日本国内で製造できる企業も少なく、世界中の供給先を探して、試薬を供給できる状態にしておく。
Q mRNAの合成を実験室レベルで行うという話があったが、合成する際の注意点はあるか?
A mRNAは分解しやすいので注意点が多々ある。PCRでコンタミネーションがあると他の遺伝子の増幅が起こる。そのため、クリーンルームで作業し、他のノイズが入らないようにしなければならないので、注意して合成していると思われる。
Q マーケティングにおける選択と集中についてどのようにされているのか?
A 試薬メーカーのリーディングカンパニーであるので、ある程度、採算を無視して品揃えをする。当社では試薬のデパートと言う感じで試薬の品揃えをする。
Q どこで利益を出すのか?
A 試薬として、希少価値があるので、手作業であれば高額の試薬もある。DNAを切る酵素がノーベル賞を受賞しているもので、かなり高額になる。
Q 世界的企業でもウイルス試薬を創薬しているが、メーカー間での相乗効果があるのか?
A そのために基礎研究が必要になり、すぐに合成できるのであれば試薬を供給できる。試薬をほしい研究者がいれば供給できる。
Q 昔は、写真メーカーが試薬を持っていた。試薬をもっているからこそ、製薬が成り立つと思うが、今後は医薬で試薬を扱うようになるのか?
A 遺伝子も含めて、新しい世界が広がったように感じている。PCRとはなにか?アデノウイルスとは何か?について知らない人が多い中で、これまでの歴史でmRNAを注射するということがなかった。今、革命が起こっている状態であると考えている。
(文責:橋本 隆幸 監修:飯塚 洋人)



